- 順天堂大学医学部附属順天堂医院
- 診療科・部門
- 診療科・外来部門
- 膠原病・リウマチ内科
- 医療関係者の⽅へ
- 対象疾患
- 悪性関節リウマチ
悪性関節リウマチ
malignant rheumatoid arthritis, MRA
一方でMRAは日本独自の疾患名・概念であり、既存のRAに中小血管炎や肺線維症、胸膜炎などの関節外症状を伴い、難治性もしくは重症の臨床病態をみとめる場合にMRAと定義され、国の指定難病となっている。疾患活動性が高く、長期罹患のRAに発症することが多い。
MRAではリウマトイド因子(rheumatoid factor, RF)高値のことが多く、免疫複合体沈着が炎症の惹起に関与していると考えられている。また、RVは、10年以上の長期罹患RAでRF陽性の男性に多く、その他に喫煙や抗環状シトルリン化ペプチド抗体(anti-cyclic citrullinated peptide antibody; anti-CCP, ACPA)高値、抗リウマチ薬多剤抵抗性などとの関連性が示されている。
鑑別診断が必要な疾患として、感染症や続発性アミロイドーシス、薬剤性の血管炎や肺・腎障害、Felty症候群や他の膠原病の合併などがある。注意点として、蕁麻疹様皮疹は薬剤や感染症、多発単神経炎はRAの関節・脊椎病変による神経症状との鑑別が必要である。
MRAの血管炎では血管造影での小動脈瘤、毛細血管炎による糸球体腎炎や肺胞出血を認めることは少なく、抗好中球細胞質抗体(antineutrophil cytoplasmic antibody, ANCA)は陰性である。可能であれば生検(皮膚、神経・筋など)を施行し、壊死性血管炎や肉芽腫性血管炎、閉塞性内膜炎を確定する。
MRAでは、RAによる多関節炎に加えて、全身性血管炎型では38℃以上の発熱、体重減少などの全身症状、および皮下結節、紫斑、上強膜炎、筋痛、間質性肺炎、胸膜炎、多発単神経炎、消化管出血などの血管炎による症状が急速に出現、悪化する。 心臓・腸管・膵臓・睾丸などの動脈炎による虚血症状や奨膜炎がみられることがある。
多発単神経炎では、手指や足趾の痺れや疼痛など知覚障害と運動障害がみられ、橈骨神経障害では下垂手(drop hand)、腓骨神経障害では下垂足(drop foot)となる。末梢動脈炎型では皮膚潰瘍、梗塞、四肢先端の壊疽、壊死がみられ、進行は通常、緩徐である。肺の間質性病変も慢性に進行することが多い。
MRAでは、関節外症状に応じて副腎皮質ステロイド等による治療を行う。皮膚症状のみであれば副腎皮質ステロイド+アザチオプリン(azathioprine, AZA)の併用療法を行い、全身症状(血管炎による臓器病変があり漿膜炎や強膜炎などの関節外病変や発熱,体重減少を伴う症例を指す。間質性肺炎のみの症例は除く)を伴う場合には副腎皮質ステロイド+シクロホスファミド(cyclophosphamide, CY)の併用療法を行う。副作用リスクが高いと考えられる場合などには、副腎皮質ステロイド単独での過量も検討する。効果不十分の場合には、CYやAZAなどの免疫抑制薬を併用する。全身性血管炎による臓器虚血・梗塞、多発単神経炎、奨膜炎、心筋炎、急性・亜急性の間質性肺炎では、プレドニゾロン換算で40〜80mg/日の経口ステロイドを投与する。緊急性や重症度により、メチルプレドニゾロンによるステロイドパルス療法を追加する。重症例ではCY 500〜1000mg、月1〜2回の静注療法を併用するが、CYは細胞毒性も強いため、血管炎が改善した段階でMTXやAZAなど他の免疫抑制薬へ変更する。
臓器虚血・梗塞や皮膚潰瘍・指端壊疽などでは、抗凝固薬や血管拡張薬を併用する。また、RFや免疫複合体が高値の場合には、血漿交換療法の併用も検討する。
RAの治療に用いられるTNFα阻害薬やIL-6阻害薬などの生物学的製剤は、未投与例においてはRAに伴う血管炎の初期や難治例における治療薬として有用である。また初期治療に対して副作用や治療抵抗性、再発性を示した症例においても投与が検討される。しかし、一方でこれらの薬剤、特にTNFα阻害薬使用下で血管炎の発症が知られており注意が必要である。リツキシマブの投与が検討されることもあるが、本邦では保険適用外である。
また、高齢者、身体機能低下例、肺線維症症例などで免疫抑制療法を行うにあたっては、ST合剤(スルファメトキサゾール・トリメトプリム合剤)の予防投与などを検討する。

疾患概念・病態
関節リウマチ(rheumatoid arthritis, RA)は関節滑膜炎と骨・軟骨破壊を特徴とするが、様々な関節外症状も伴う。RAに中型・小型の血管炎を伴う場合に欧米ではリウマトイド血管炎(rheumatoid vasculitis, RV)と呼ばれている。一方でMRAは日本独自の疾患名・概念であり、既存のRAに中小血管炎や肺線維症、胸膜炎などの関節外症状を伴い、難治性もしくは重症の臨床病態をみとめる場合にMRAと定義され、国の指定難病となっている。疾患活動性が高く、長期罹患のRAに発症することが多い。
MRAではリウマトイド因子(rheumatoid factor, RF)高値のことが多く、免疫複合体沈着が炎症の惹起に関与していると考えられている。また、RVは、10年以上の長期罹患RAでRF陽性の男性に多く、その他に喫煙や抗環状シトルリン化ペプチド抗体(anti-cyclic citrullinated peptide antibody; anti-CCP, ACPA)高値、抗リウマチ薬多剤抵抗性などとの関連性が示されている。
疫学
MRAはRA患者の0.6〜1.0%にみられるとされ、平成25年度の医療受給者証保持者は6,433人、平成30年度では5,406人であった。診断時の年齢のピークは60歳代で、男女比は1:2である。血管炎による内臓病変や間質性肺炎を有すると生命予後は不良である。診断・鑑別診断
MRAの診断には、表に示す診断基準が用いられる(厚生労働省ホームページ、悪性関節リウマチ、概要・診断基準等)。鑑別診断が必要な疾患として、感染症や続発性アミロイドーシス、薬剤性の血管炎や肺・腎障害、Felty症候群や他の膠原病の合併などがある。注意点として、蕁麻疹様皮疹は薬剤や感染症、多発単神経炎はRAの関節・脊椎病変による神経症状との鑑別が必要である。
MRAの血管炎では血管造影での小動脈瘤、毛細血管炎による糸球体腎炎や肺胞出血を認めることは少なく、抗好中球細胞質抗体(antineutrophil cytoplasmic antibody, ANCA)は陰性である。可能であれば生検(皮膚、神経・筋など)を施行し、壊死性血管炎や肉芽腫性血管炎、閉塞性内膜炎を確定する。
臨床症状
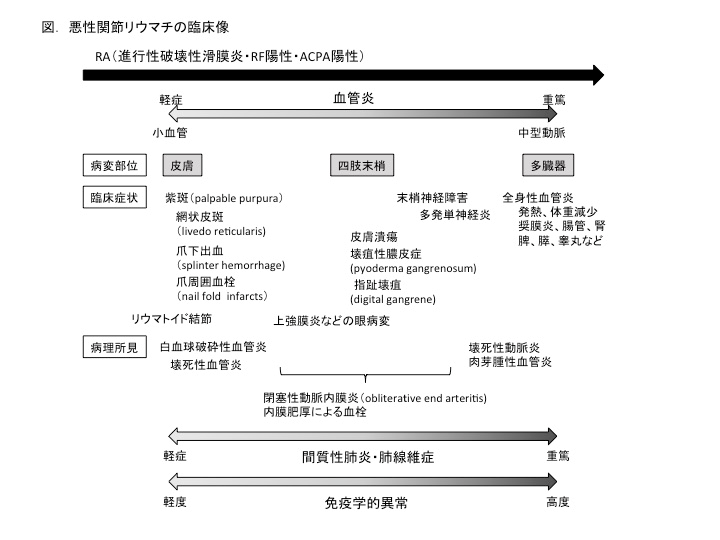
MRAの臨床像を図に示す。血管炎は、結節性多発動脈炎(polyarteritis nodosa, PAN)に類似する全身性血管炎型(内臓を系統的に侵し、生命予後不良)と、内膜の線維性増殖を呈する末梢動脈炎型(四肢末梢及び皮膚を侵し、生命予後は良好)に分けられる。また、その他に間質性肺炎や肺線維症が主体の肺臓炎型がある。MRAでは、RAによる多関節炎に加えて、全身性血管炎型では38℃以上の発熱、体重減少などの全身症状、および皮下結節、紫斑、上強膜炎、筋痛、間質性肺炎、胸膜炎、多発単神経炎、消化管出血などの血管炎による症状が急速に出現、悪化する。 心臓・腸管・膵臓・睾丸などの動脈炎による虚血症状や奨膜炎がみられることがある。
多発単神経炎では、手指や足趾の痺れや疼痛など知覚障害と運動障害がみられ、橈骨神経障害では下垂手(drop hand)、腓骨神経障害では下垂足(drop foot)となる。末梢動脈炎型では皮膚潰瘍、梗塞、四肢先端の壊疽、壊死がみられ、進行は通常、緩徐である。肺の間質性病変も慢性に進行することが多い。
治療
メトトレキサート(methotrexate, MTX)を中心とした抗リウマチ薬(disease modified anti rheumatic drugs, DMARDs)にてRAの疾患活動性自体をよくコントロールし、寛解もしくは低疾患活動性を達成し維持することがMRAの発症や増悪を防ぐために重要である。MRAでは、関節外症状に応じて副腎皮質ステロイド等による治療を行う。皮膚症状のみであれば副腎皮質ステロイド+アザチオプリン(azathioprine, AZA)の併用療法を行い、全身症状(血管炎による臓器病変があり漿膜炎や強膜炎などの関節外病変や発熱,体重減少を伴う症例を指す。間質性肺炎のみの症例は除く)を伴う場合には副腎皮質ステロイド+シクロホスファミド(cyclophosphamide, CY)の併用療法を行う。副作用リスクが高いと考えられる場合などには、副腎皮質ステロイド単独での過量も検討する。効果不十分の場合には、CYやAZAなどの免疫抑制薬を併用する。全身性血管炎による臓器虚血・梗塞、多発単神経炎、奨膜炎、心筋炎、急性・亜急性の間質性肺炎では、プレドニゾロン換算で40〜80mg/日の経口ステロイドを投与する。緊急性や重症度により、メチルプレドニゾロンによるステロイドパルス療法を追加する。重症例ではCY 500〜1000mg、月1〜2回の静注療法を併用するが、CYは細胞毒性も強いため、血管炎が改善した段階でMTXやAZAなど他の免疫抑制薬へ変更する。
臓器虚血・梗塞や皮膚潰瘍・指端壊疽などでは、抗凝固薬や血管拡張薬を併用する。また、RFや免疫複合体が高値の場合には、血漿交換療法の併用も検討する。
RAの治療に用いられるTNFα阻害薬やIL-6阻害薬などの生物学的製剤は、未投与例においてはRAに伴う血管炎の初期や難治例における治療薬として有用である。また初期治療に対して副作用や治療抵抗性、再発性を示した症例においても投与が検討される。しかし、一方でこれらの薬剤、特にTNFα阻害薬使用下で血管炎の発症が知られており注意が必要である。リツキシマブの投与が検討されることもあるが、本邦では保険適用外である。
また、高齢者、身体機能低下例、肺線維症症例などで免疫抑制療法を行うにあたっては、ST合剤(スルファメトキサゾール・トリメトプリム合剤)の予防投与などを検討する。
予後
MRAの予後は、軽快21%、不変26%、悪化31%、死亡14%、不明・その他8%との疫学調査成績があり、死因は呼吸不全が最も多く、次いで感染症の合併、心不全、腎不全などである。RVの欧米における報告では、最近のRA治療の進歩に伴い発症頻度は低下傾向にあるが、死亡率に変化はないことが示されている。
